- гипертоническая болезнь
- ишемическая болезнь сердца
- аритмии
- сердечная недостаточность
- пневмония
- бронхиальная астма
- аллергия
- терапевтическая стоматология
- хирургическая стоматология
- ортопедическая стоматология
- удаление зубного камня
- профессиональная система отбеливания зубов «ZOOM»
- грыжа межпозвонкового диска
- повреждения грудного и поясничного отдела позвоночника
- повреждения шейного отдела позвоночника
- поражение позвоночника при остеопорозе
- спондилолистез
Современные подходы к лечению осложненной костной раны
СОВРЕМЕННЫЕ ПОДХОДЫ К ЛЕЧЕНИЮ ОСЛОЖНЕННОЙ КОСТНОЙ РАНЫ
Просвирин А.А., Склянчук Е.Д., Гурьев В.В., Шаповал А.И., Щепилов Д.В., Митяев Д.В., Яхьяев В.Д., Сергеев А.А.
Введение. Известно, что причиной развития и рецидивирующего течения остеомиелита являются стойкие нарушения микроциркуляции и нарушение репаративных процессов, связанных с тяжестью повреждений, ослабление общего и местного иммунитета создающие условия для присоединения патологической микрофлоры. По данным научной литературы хронический остеомиелит в общей структуре заболеваний опорно-двигательного аппарата составляет 12-25% [1,3,5,8,9]. Вероятность его развития после хирургического лечения открытых переломов составляет 21-46,2%, а после закрытых переломов 7,6-13,2% [7,10]. Учитывая, что до 80% этих больных представлены лицами молодого, работоспособного возраста и преимущественно мужчинами, проблема лечения хронического остеомиелита является не только медицинской, но и социальной.
Лечение хронического рецидивирующего остеомиелита длинных костей, или воспаления костного мозга, обычно распространяющегося на компактное и губчатое вещество кости и надкостницу независимо от этиологии и клинического течения имеет общие принципы. Таковыми являются вскрытие гнойных очагов, секвестрнекрэктомия, промывание очага антисептическими растворами, заполнение образовавшихся костных дефектов, антибактериальная терапия.
С учетом исключительной сложности лечения остеомиелита с высоким процентом неудовлетворительных результатов один из ведущих специалистов по данной проблеме George Cierny (США) популяризировал концепцию лечения остеомиелита по аналогии с лечением опухолей костей, согласно которой очаг остеомиелита должен удаляться единым блоком, как в костной онкологии [11]. Однако такой подход приводит к образованию сегментарного дефекта кости с полным нарушением опороспособности конечности и создает большие сложности в последующем восстановлении ее целостности.
Известно, что одним из механизмов возникновения рецидива хронического остеомиелита является остеонекроз, некроз костной ткани вместе с содержимым ее каналов и полостей, который преимущественно имеет остроишемический генез [4]. В условиях патологических изменений, развивающихся в кости на достаточно большом протяжении вокруг непосредственно самого остеомиелитического очага при длительно протекающем гнойно-воспалительном процессе и характеризующихся высокой склеротической плотностью костных тканей, обедненных сосудами, вероятность развития ишемического остеонекроза повышается многократно. Небольшие очаги, без присоединения инфекции, способны в ходе остеокластической резорбции к самоперестройке и реоссификации. Более крупные, особенно при присоединении инфекции подвергаются гнойному расплавлению с образованием секвестров и прорывом содержимого наружу с формированием свищей.
Вторым по значимости механизмом развития рецидивов гнойно-некротического заболевания костей является наличие остаточной полости и вяло текущей инфекции.
Для пластики образующихся костных дефектов применяются различные способы, среди которых наиболее широкое распространение получила транспозиция мышечных лоскутов, что создает хорошие условия для реваскуляризации остеомиелитического очага и обеспечивает равномерное заполнение костной полости стойкими к инфекции васкуляризированными тканями. Однако мышечная пластика имеет ряд существенных недостатков, связанных, во-первых, с тем, что мышечная ткань в костной полости рубцово перерождается и препятствует регенерации кости в зоне дефекта, во-вторых, с естественным ограничением аутогенного пластического материала.
В качестве альтернативы известны способы пластики остаточных полостей аутогенными, аллогенными и ксеногенными тканями и имплантатами [2,6,8], например, измельченным формалинизированным хрящом [1]. Однако, как и мышечная пластика, эти способы также имеют ряд существенных недостатков, связанных с ограничением пластического материала, усложнением и повышением травматичности операции. В то же время, свободный костный трансплантат, несомненно, обладая наилучшими остеоиндуктивными и остеокондуктивными свойствами, активизируя репаративный процесс, все же в ходе репаративной регенерации закономерно резорбируется с замещением новообразующейся костной тканью. При этом, в случае наличия неудовлетворительных условий для остеогенного течения регенерации, его потенций зачастую оказывается недостаточно, и он, рассасываясь, замещается фиброзно-хрящевой мозолью. Кроме того, в костной ране остеомиелитического очага, будучи аваскулярным объектом, трансплантат может стать хорошей питательной средой для бактериальной флоры, и как следствие вызвать обострение остеомиелитического процесса.
Цель исследования: восстановление целостности кости в патологических посттравматических условиях, препятствующих остеогенному течению репаративных процессов.
Материалы и методы. Разработка способа этиотропного хирургического лечения остеомиелита осуществлена на основе анализ результатов лечения 1378 больных с посттравматическим остеомиелитом костей конечностей, среди которых поражение бедра имело место в 380 случаях, таза в 85, голень 745, верхней конечности – 168. Оценка остеогенности материала in vivo проводилась на модели ортотопической имплантации, выполненной на 17 половозрелых крысах линии Wistar. У каждого животного под внутримышечным наркозом растворами Zooxylasin и Zoletil 100 в костях черепа трепаном диаметром 3,5 мм, формировались два костных дефекта. Опытный дефект заполняли подготовленным имплантатом, контрольный – оставляли свободным. На сроках 1, 4 и 8 недель проводилось гистологическое исследование эксплантированного материала с окраской срезов по Ван-Гизону и гематоксилин-эозином.
Результаты и обсуждение. Анализ развития рецидивов остеомиелитического процесса после санирующих операций показал, что в основе рецидивирующего течения заболевания лежит формирование зоны остеонекроза в массе патологически измененных гиповаскулярных костных тканей как инфекционной, так и асептической природы.
С учетом полученных результатов, характеризующих патогенез рецидивирующего течения остеомиелита, был разработан способ хирургического лечения, при котором задача оптимизации регенерации достигается резекцией разрушенной части 1 кортикального слоя кости 2 в пределах непораженных гнойно-деструктивным процессом костных тканей 3 с удалением костных секвестров 4 (рис.1), а через образовавшийся пострезекционный костный дефект 5 под визуально-рентгенологическим контролем производят резекцию всей внутренней части склеротически измененной костной ткани 6 в пределах опорной части 7 кортикального слоя кости 2 со вскрытием костномозгового канала 8 (рис.2).
Вместо резекции, оставшиеся склерозированные костные ткани 7 кортикального слоя кости 2, сохраняющие непрерывность и опороспособность кости, изнутри через пострезекционный кортикальный костный дефект 5 со стороны пострезекционной интрамедуллярной костной полости 10 перфорируют на всем их протяжении, создавая множественные сквозные отверстия 11 (рис.3).
Сквозные перфорационные отверстия 11 наносят равномерно в плоскости кости с минимальным диаметром в зависимости от толщины перфорируемой кости таким образом, чтобы сформировать мелкоячеистую костную структуру без потери ее опорной целостности с равным распределением в объеме кости одинаковых по размеру сквозных пустот отверстий 11 и окружающей сети костных промежутков 12, что ограничивает возможность ползущего распространения очагов остеонекроза в костной ткани и уменьшает общую склеротическую плотность патологически измененного опорного кортикального слоя кости 7 (рис.4).
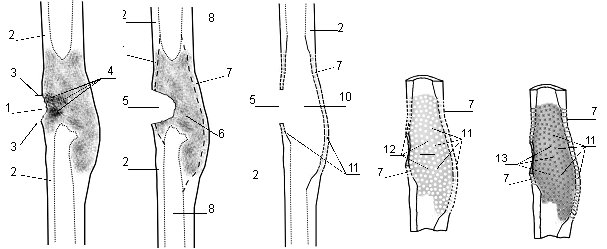
Рис.1 Рис.2 Рис.3 Рис.4 Рис.5
Для повышения механической прочности перфорированного опорного кортикального слоя 7 с созданием пролонгированной антибактериальной среды и активизацией костных репаративных процессов все пространства перфорационных отверстий 11 заполняют интраоперационно затвердевающим бактерицидным костно-пластическим материалом 13 (рис.5).
Миниинвазивно транскутантно под рентгенологическим контролем трепанируют кость 14 в пределах неизмененных костных тканей и в интрамедуллярное костное пространство 10 устанавливают две дренажные трубки 15 для проточно-промывной системы и производят пластику пострезекционного дефекта 5 в кортикальном слое кости 2 (рис.6) интраоперационно затвердевающим бактерицидным костно-пластическим материалом 16, который затвердевая в дефекте, герметизирует интрамедуллярную костную полость 10 и восстанавливает целостность и механическую прочность кортикального слоя кости 2 на этом ослабленном участке (рис.7). Рана промывается антисептиками, послойно наглухо ушивается.
В послеоперационном периоде на фоне общей антибиотикотерапии проводят проточно-промывное дренирование интрамедуллярной костной полости с использованием антисептиков и активизирующих репаративные процессы лекарственных препаратов в условиях закрытой стерильной системы.
После ликвидации операционного травматического воспаления и очищения выделяющегося промывного раствора через одну из трубок 15 дренажной системы вводят эндоскоп 17 и контролируют развитие грануляционных тканей 18 на стенках эндостальной костной полости 10 и при их созревании без повторного хирургического вмешательства в асептических условиях под эндовизуальным контролем эндоскопом 17 вводят бактерицидный остеогенный костнопластический материал 19 через вторую дренажную трубку 15 (рис.8). После равномерного заполнения костной полости костно-пластическим материалом 19 эндоскоп и дренажные трубки через трепанационные отверстия 14 в кортикальном слое кости 2 удаляют (рис.9).
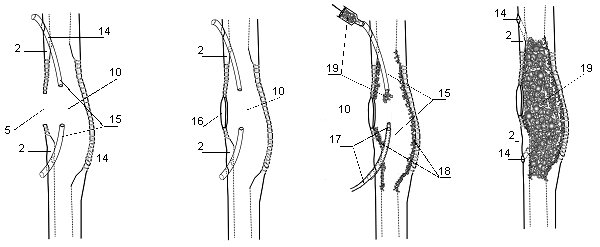
Рис.6 Рис.7 Рис.8 Рис.9
При клинической апробации способа получен положительный результат с ликвидацией гнойно-некротического процесса в кости и с отсутствием рецидивов заболевания в течение 3-х летнего периода наблюдения.
Для решения вопроса замещения осложненных костных полостей нами был разработан новый пористый коллаген-апатитный материал. При гистологическом анализе результатов через два месяца ортотопической имплантации материала констатируется более выраженное уменьшение диаметра опытного дефекта теменных костей 1 за счет увеличения «конуса костного роста» (а), по сравнению с контрольным дефектом 2 (рис.10А). В опытном дефекте с имплантированным материалом отмечаются активные репаративные процессы с резорбцией материала до 30% его исходного объема.
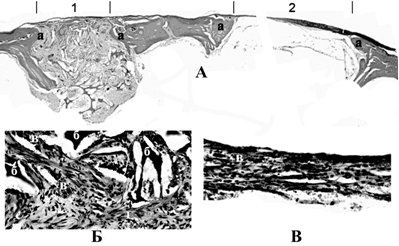
Рис. 10. Гистологические результаты ортотопической имплантации материала (срок 8 недель после формирования дефектов в теменных костях черепа крысы)
А – гистотопограмма, окраска по Ван-Гизону, х4 (1 – опытный дефект с имплантированным материалом, 2 – контрольный дефект); Б – центральная часть регенерата в опытном дефекте, окраска гематоксилином и эозином, х400; В – центральная часть регенерата в контрольном дефекте, окраска гематоксилином и эозином, х200. (а– ретикулофиброзная костная ткань регенерата («конус костного роста»), б– участки имплантированного материала, в– кровеносные сосуды, г– строящаяся волокнистая ткань).
Вокруг остающихся участков материала (б) отсутствуют признаки образования соединительнотканной капсулы или лейкоцитарного вала, наблюдается множество кровеносных сосудов (в) в активно строящейся волокнистой соединительной ткани (г) (рис.10Б). В контрольных дефектах не обнаруживается значимых признаков остеогенеза, меньше сосудов, дефект заполняется тонкой перепонкой соединительнотканного строения (рис.10В).
Выводы: 1) разработанный костный имплантат обладает свойствами, активизирующими репаративные процессы кости; 2) в сочетании с разработанной хирургической технологии лечения новый костно-пластический материал может обеспечить восстановление целостности кости в патологических посттравматических условиях, препятствующих остеогенному течению репаративных процессов.
Список литературы.
- Авторское свидетельство СССР № 700115, A61B17100, 1979 г.
- Азолов В.В., Александров Н.М., Алейников А.В. Использование лоскутов с осевым кровоснабжением для устранения обширных костно-мягкотканых дефектов конечностей в условиях измененного реципиентного ложа. //Тезисы докладов VII съезда травматологов-ортопедов России. – Новосибирск, 2002. – Т.1 – С.378-379.
- Батаков Е.А., Ишутов И.В. Современные аспекты комплексного лечения хронического остеомиелита. //Казанский медицинский журнал. – 2008. – Т. 89, № 1. – С.41-43.
- Григоровский В.В. Современные представления о патологии и патанатомии гематогенного остеомиелита и их значение для клинической практики. //Международный медицинский журнал. – 2003. – №1. – С.104-108.
- Ерюхин И.А., Гельфанд Б.Р., Шляпников С.А. Хирургические инфекции: практическое руководство. – М.: Литтера, 2006. – 736 с.
- Каплан А.В., Махсон Н.Е., Мельникова В.М. //Гнойная травматология костей и суставов. – М.: Медицина, 1985. – 384 с.
- Кононов В.С. Гематогенный остеомиелит у детей". – М.: Медицина, 1974.
- Никитин Г.Д., Рак А.В., Линник С.А. и др. //Хирургическое лечение остеомиелита. – Санкт-Петербург, 2000. – 287 с.
- Оноприенко Г.А., Буачидзе О.Ш., Еренин А.В., Савицкая К.И. и др. Хирургическое лечение больных с хроническим гнойным поражением костей и крупных суставов конечностей. //Хирургия. – 2005. – №8. – С.29-35.
- Соколов В.А. Множественные и сочетанные травмы. – М.: ГОЭТАР-Медиа, 2006. – 512 с.
- Cierny G. Chronic osteomyelitis: Results of treatment. //Instr. Course Lect. – 1990. – 1: 39 – P.495-508.
- Приемное отделение
- Нейрохирургическое отделение
- Хирургическое отделение
- Отделение гнойной хирургии
- Отоларингологическое отделение
- Гинекологическое отделение
- Гастроэнтерологическое отделение
- Пульмонологическое отделение
- Эндокринологическое отделение
- Кардиологическое отделение
- Неврологическое отделение
- Отделение анестезиологии и реанимации
- Восстановительное лечение
- Пластическая хирургия
- Отделение повышенной комфортности
- Отделение диализа
- Отделение скорой
медицинской помощи - Отделение рентгенохирургических методов диагностики и лечения
- Поликлиника на ст. Люблино
- Стоматологическое отделение
- Кабинет медицинского психолога
- Терапевтическое отделение №1
- Кабинет психиатра-нарколога
- Терапевтическое отделение №2
- Кабинет психотерапевта
- Женская консультация
- Кабинет по раннему выявлению заболеваний молочной железы
- Подологический кабинет (медицинский маникюр, педикюр)
- Кабинет терапевтической косметологии
- Консультативно-диагностический центр
- Центр экспертизы профессиональной пригодности
- Лаборатория клинической андрологии
2024© semashko.com
ЧУЗ “КБ ”РЖД-Медицина” им Н.А. Семашко” использует cookie. Файлы cookie хранят полезную информацию на вашем компьютере для того, чтобы мы могли улучшить оперативность и точность нашего сайта для вашей работы. В некоторых случаях файлы cookie необходимы для обеспечения корректной работы сайта. Вы можете запретить сохранение cookie в настройках своего браузера.
Ознакомьтесь с политикой конфиденциальности.
Создание сайтов - Medafarm STUDIO











 Независимая оценка качества условий оказания услуг медицинскими организациями
Независимая оценка качества условий оказания услуг медицинскими организациями Департамент здравоохранения города Москвы
Департамент здравоохранения города Москвы Официальный сайт для размещения информации о государственных (муниципальных) учреждениях
Официальный сайт для размещения информации о государственных (муниципальных) учреждениях Московская межрегиональная транспортная прокуратура
Московская межрегиональная транспортная прокуратура Федеральная служба по надзору в сфере здравоохранения
Федеральная служба по надзору в сфере здравоохранения


